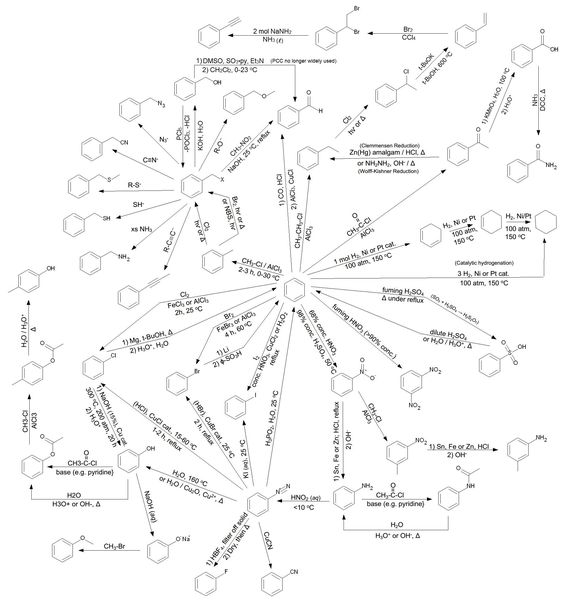
Giới thiệu công thức hóa hữu cơ
Hóa hữu cơ tập trung vào cấu trúc, tính chất, thành phần, phản ứng và chuẩn bị các hợp chất chứa cacbon. Việc hiểu công thức của các hợp chất hữu cơ là điều cần thiết để thành công trong các khóa học hóa hữu cơ và các nghề nghiệp trong tương lai liên quan đến hóa học, hóa sinh, kỹ thuật hóa học, dược lý và y khoa.
Đặt tên các hợp chất hữu cơ
Hệ thống danh pháp IUPAC (Liên minh Hóa học Thuần túy và Ứng dụng Quốc tế) được sử dụng để đặt tên các hợp chất hữu cơ dựa trên cấu trúc và thành phần của chúng. Bằng cách học các quy tắc đặt tên IUPAC, bạn có thể dễ dàng giải thích công thức của các hợp chất hữu cơ.
Các loại hợp chất hữu cơ
Có một số nhóm hợp chất hữu cơ chính mà bạn sẽ thường gặp:
- Hydrocacbon - bao gồm các nguyên tử cacbon và hiđrô
- Haloankan - hydrocacbon với các thế thay thế halogen
- Rượu và phenol - chứa nhóm -OH
- Ete - chứa một nguyên tử ôxy nối với hai chuỗi cacbon
- Andehit và xeton - chứa nhóm cacbony
- Axit cacboxylic - chứa nhóm cacboxy (-COOH)
- Este và amit - bắt nguồn từ axit cacboxylic
- Amin - chứa nitơ
Vẽ cấu trúc và công thức
Một số nguyên tắc chính để vẽ các cấu trúc hữu cơ:
- Các nguyên tử cacbon là các nguyên tử trung tâm trong hầu hết các hợp chất hữu cơ
- Các đường thẳng đại diện cho liên kết giữa các nguyên tử
- Các nguyên tử cacbon ở đầu mặt được hiểu là có hydrogen liên kết
- Các nhóm chức quyết định các tính chất và phản ứng
Các loại phản ứng chính
Việc hiểu các dạng phản ứng chung với các hợp chất hữu cơ cho phép bạn hiểu rõ hơn các chuyển hóa và quá trình biến đổi.
Thế
Phản ứng thế liên quan đến việc thay thế một nguyên tử/nhóm bằng một nguyên tử/nhóm khác. Ví dụ:
CH3CH2Br + OH- → CH3CH2OH + Br-
Loại bỏ
Phản ứng loại bỏ liên quan đến việc loại bỏ các nguyên tử/nhóm và hình thành các liên kết đôi hoặc ba. Ví dụ:
CH3CHBrCH3 → CH2=CHCH3 + HBr
Bổ sung
Phản ứng bổ sung liên quan đến việc bổ sung các nguyên tử xuyên qua các liên kết đôi hoặc ba. Ví dụ:
CH2=CH2 + HBr → CH3CH2Br
Các điều kiện phản ứng quan trọng
Việc hiểu các điều kiện khác nhau ảnh hưởng đến phản ứng cho phép bạn dự đoán các sản phẩm và tối ưu hóa hiệu suất.
Axit và bazơ
Sự có mặt của axit hoặc bazơ có thể thay đổi đáng kể các con đường thế/loại bỏ. Axit mạnh thúc đẩy phản ứng loại bỏ trong khi bazơ mạnh thúc đẩy phản ứng thế.
Chất oxy hóa so với chất khử
Sự giàu điện tử của các chất phản ứng ảnh hưởng đến cơ chế phản ứng. Chất oxy hóa loại bỏ điện tử, trong khi chất khử hiến tặng điện tử.
Nhiệt độ và ánh sáng
Tăng năng lượng nhiệt hoặc chiếu tia cung cấp năng lượng để vượt qua các rào cản kích hoạt và đẩy nhanh các phản ứng.
Luyện tập với công thức hóa hữu cơ
Để thành thạo ký hiệu viết tắt các đường và ký hiệu đòi hỏi sự luyện tập. Hãy làm qua nhiều ví dụ về vẽ/giải thích các cấu trúc và thiết lập cơ chế phản ứng.
Ghi nhớ các nhóm chức
Hãy nắm vững các nhóm chức phổ biến như halogen ankan, rượu, amin, axit cacboxylic, andehit, xeton và cách viết tắt của chúng.
Bắt đầu từ những cấu trúc đơn giản
Luyện tập vẽ và đặt tên cho các ankan đơn chuỗi thẳng trước khi chuyển sang các cấu trúc phức tạp hơn như vòng và thơm.
Sử dụng mô hình
Các bộ mô hình vật lý với liên kết và nguyên tử có thể giúp hình dung các hình dạng và cấu trúc 3D.